jueves, 31 de enero de 2019
FUKUSHIMA
El día 11 de marzo de 2011 se produjo un accidente nuclear en el suroeste de Japón en una ciudad llamada Fukushima. Todo empezó por un terremoto de magnitud 9,0 el cuál desencadenó un tsunami con olas que llegaban a los 40,5 metros de altura y el tsunami dañó gravemente la central nuclear Fukushima Dahiichi, de 6 reactores solo habían 3 reactores operando los cuales dejaron de funcionar después del terremoto y al no poder enfriarlos con energía eléctrica los reactores se sobrecalentaron, para evitarlo usaron motores diésel para generar energía eléctrica pero estos dejaron de funcionar por culpa del tsunami lo que causó una fusión del núcleo en los 3 reactores. Al final entre el tsunami y la explosión de la central nuclear murieron 18498 personas y 3088 personas han muerto por culpa de enfermedades de aquel día y ha contaminado el océano más grande del mundo en solo cinco años y aún continúan escapándose 300 toneladas de desechos radioactivos cada día.
El acido sulfúrico (Formula, usos y propiedades)
¿Qué es el ácido sulfúrico?
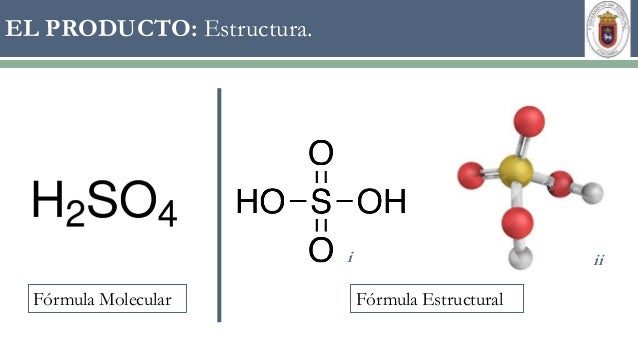
El ácido sulfúrico (H2SO4) o sulfato de hidrógeno, es un líquido incoloro, viscoso y un ácido inorgánico fuerte. Es un ácido mineral y es uno de los 20 productos químicos más importantes en la industria química. Como aditivo alimentario tiene el número E 513. Hasta el siglo XIX, el ácido sulfúrico también tenía el nombre trivial de aceite de vitriolo, que ya no se utiliza hoy en día.
Ácido sulfúrico fórmula
La fórmula química del ácido sulfúrico es H2SO4 y su peso molecular es de 98.079 g/mol. Su estructura química se muestra a continua.
Peligros para la salud
El ácido sulfúrico no es, por sí solo, un producto químico doméstico común debido al peligro que conlleva su manipulación.
El concentrado de H2SO4 es altamente corrosivo y puede dañar severamente los tejidos al contacto. Al ser un ácido fuerte, oxidante, agente corrosivo y deshidratante, es más peligroso que los otros ácidos minerales. Causa quemaduras químicas severas al contacto con la piel. El contacto con los ojos puede causar daño permanente y ceguera.
Incluso la cantidad más pequeña puede causar quemaduras graves si entra en contacto con la piel, mientras que respirar el gas liberado por las reacciones con otras sustancias puede causar dificultad para respirar y una sensación de ardor en el sistema respiratorio.
Aunque no hay riesgo de incendio o explosión con ácido sulfúrico solamente, es altamente combustible cuando se combina con muchos otros materiales y tipos de materia orgánica, así como con agua. Además de las quemaduras, las personas expuestas directamente al ácido sulfúrico pueden entrar en shock si se ingiere alguno de los productos químicos; se debe buscar atención médica inmediatamente si esto ocurre.
Ácido Sulfúrico quemadura
Una quemadura de ácido sulfúrico es una emergencia médica y requiere tratamiento inmediato. El primer y más importante paso es diluir y eliminar todo el ácido sulfúrico en el lugar de la quemadura irrigando abundantemente con agua. El ácido sulfúrico continuará quemándose en la piel hasta que sea removido. Toda la ropa o equipo con ácido sulfúrico también debe ser removido por una persona que use equipo de protección.
Las quemaduras químicas, como las causadas por el ácido sulfúrico, pueden ocurrir en varios lugares, principalmente en entornos industriales. Sin embargo, el ácido sulfúrico se encuentra en algunos productos domésticos. Todos los productos químicos del hogar deben guardarse bajo llave, fuera del alcance de los niños.
Ácido sulfúrico propiedades
El ácido sulfúrico con la fórmula de suma H2SO4 es un ácido fuerte (pKS1 = -3, pKS2, que corresponde al pKS del anión sulfato de hidrógeno HSO4- = 1,9). Como ácido inorgánico fuerte pertenece a los ácidos minerales.
El ácido sulfúrico concentrado es también un poderoso agente oxidante. También tiene un efecto higroscópico, por lo que puede utilizarse para el secado de gases y líquidos. La molécula de ácido sulfúrico tetraédrico distorsionado tiene un gran momento dipolo, cuyo polo positivo se encuentra entre los dos grupos OH.
Junto con el agua, el ácido sulfúrico forma un azeotrópico. Si el ácido sulfúrico al 100 % se calienta hasta el punto de ebullición, el trióxido de azufre se evapora hasta alcanzar una concentración de aproximadamente el 98 % en peso. Por el contrario, el ácido sulfúrico diluido puede reducirse a esta concentración hirviéndolo.
Ácido sulfúrico concentrado
El ácido sulfúrico al 100 % se produce introduciendo trióxido de azufre en aproximadamente un 98 % de ácido sulfúrico en peso hasta que sea anhidro. El ácido sulfúrico también puede aglutinar el trióxido de azufre en grandes cantidades, por lo que el líquido resultante se denomina óleum, ya que la viscosidad es bastante alta. El óleo consiste en una mezcla de ácido sulfúrico y ácidos polisulfúricos (ácido di-sulfúrico: H2S2O7, ácido trisulfúrico H2S3O10, etc.) En el comercio hay óleo con hasta un 65% en peso de trióxido de azufre. El óleo se utiliza en reacciones químicas para la sulfonación o cuando es necesario ligar tanta agua como sea posible de la reacción. Esto minimiza el consumo de ácido sulfúrico y a menudo también maximiza el rendimiento.
Para determinar la concentración, se mide la densidad del ácido sulfúrico. Puede utilizar tablas estándar para sacar una conclusión directa sobre la concentración. Por ejemplo, se determina el estado de carga de una batería de coche.
Al diluir ácido sulfúrico concentrado, se libera mucho calor. Por lo tanto, deben tomarse las precauciones adecuadas. Es importante que el ácido se añada siempre al agua, no al agua del ácido! De lo contrario, puede producirse una evaporación explosiva del agua que provoque salpicaduras incontroladas del líquido; el peligro es evidente.
Propiedades físicas
- H2SO4 es un líquido viscoso incoloro o ligeramente amarillo con un olor penetrante.
- Tiene una densidad de 1,84 g/mL
- Punto de ebullición de 337 °C
- Punto de fusión de 10 °C.
El ácido sulfúrico “concentrado” es 98% en agua, y es la forma más estable. Muchas otras concentraciones, con diferentes nombres, están disponibles para varios propósitos. El ácido de la batería es del 29-32%, el ácido de la cámara es del 62-70%, y el ácido de la torre es del 78-80%.
Propiedades químicas
El ácido sulfúrico es un ácido diprótico muy fuerte. Es higroscópico y absorbe fácilmente la humedad del aire. Es un poderoso agente oxidante y reacciona con muchos metales a altas temperaturas. Concentrado H2SO4 es también un agente deshidratante fuerte. La adición de agua al ácido sulfúrico concentrado es una reacción muy exotérmica y puede provocar explosiones.
Usos del ácido sulfúrico
El ácido sulfúrico es uno de los productos químicos más frecuentemente producidos. En 1997, se produjeron más de 130 millones de toneladas en todo el mundo. Las posibilidades de aplicación son muy variadas. Se utiliza ácido sulfúrico
- Descomposición de minerales (por ejemplo, titanio (IV)-óxido o digestión de uranio)
- Producción de sulfatos
- Preparación de otros ácidos (por ejemplo, ácido fluorhídrico o ácido fosfórico)
- Producción de abonos mediante ácido nítrico
- Producción de tensioactivos
- como catalizador
- para el tratamiento de metales
- como desecante
- como ayuda de reacción (ácido nítrico)
- en baterías de coche
- para grabado de semiconductores
- debido a su conductividad como aditivo para el agua durante la electrólisis
- como disolvente durante el ahumado
- en analítica para determinar los números de viscosidad de la poliamida
- para la producción de dióxido de titanio
En la industria alimentaria, el ácido sulfúrico se utiliza como coadyuvante técnico para la producción de almidón y caseína, y para el tratamiento del agua potable. No influye en el producto final y, por lo tanto, no está presente o sólo en trazas inocuas para la salud. En la Unión Europea, el ácido sulfúrico no tiene que estar etiquetado en el envase del producto.
Disolver el permanganato de potasio en ácido sulfúrico hasta que la saturación resulta en un líquido aceitoso de color verde oscuro (dimanganeso heptóxido) que es un agente oxidante fuerte. Carboniza los materiales orgánicos como la madera de forma inmediata y espontánea con acetona u otros combustibles. Al disolver el dicromato de potasio en ácido sulfúrico, se obtiene el ácido cromosulfúrico, un agente que antes se utilizaba con frecuencia en laboratorios para fines de limpieza.
La cantidad de ácido sulfúrico producido fue un indicador del desempeño de la industria química de un país. En la segunda fase de desarrollo de la industria química se consumen grandes cantidades de ácido sulfúrico.
Obtención del ácido
El ácido sulfúrico solía producirse mediante el proceso del vitriolo y el proceso de la cámara de plomo. Los métodos modernos son el método de contacto y el método de doble contacto resultante.
El proceso más antiguo para la producción de ácido sulfúrico es el proceso del vitriolo. Fue utilizado por los alquimistas en el siglo XIII. Los nitroles son sulfatos que pueden descomponerse térmicamente con relativa facilidad, convirtiéndose en trióxido de azufre y óxido metálico. Johann Rudolph Glauber (1604-1670) construyó la primera fábrica de ácido sulfúrico del mundo, que produjo ácido sulfúrico en Nordhausen (resina) utilizando este proceso alrededor de 1650.
En el proceso de contacto, la producción se lleva a cabo en tres etapas, en las que el dióxido de azufre (SO2) está representado en primer lugar por azufre elemental (S) y oxígeno (O2)
Historia del ácido sulfúrico
Aunque el ácido sulfúrico es ahora uno de los productos químicos más utilizados, probablemente era poco conocido antes del siglo XVI. Fue preparado por Johann Van Helmont (c. 1600) mediante la destilación destructiva de vitriol verde (sulfato ferroso) y la quema de azufre. La primera gran demanda industrial importante de ácido sulfúrico fue el proceso Leblanc para fabricar carbonato de sodio (desarrollado en 1790). El ácido sulfúrico se producía en Nordhausen a partir de vitriolo verde, pero era caro. Johann Glauber utilizó por primera vez en el siglo XVII un proceso para su síntesis quemando azufre con salitre (nitrato de potasio). y desarrollado comercialmente por Joshua Ward en Inglaterra hacia 1740. Pronto fue reemplazado por el proceso de la cámara de plomo, inventado por John Roebuck en 1746 y desde entonces mejorado por muchos otros. El proceso de contacto fue desarrollado originalmente por Peregrine Phillips en Inglaterra en el año 1830; se utilizó poco hasta que surgió la necesidad de ácido concentrado, particularmente para la fabricación de colorantes orgánicos sintéticos.
a
miércoles, 30 de enero de 2019
Chernóbil
El accidente de Chernóbil fue un accidente nuclear sucedido en la central nuclear Vladímir llich lenin, la catástrofe ocurrió en Ucrania el 26 de abril de 1986. Fue considerado como el accidente nuclear más grave en la Escala Internacional de Accidentes Nucleares. Aquel día se simulaba una prueba en la que se simulaba un corte de suministro eléctrico, un aumento súbito de potencia en el reactor 4 produjo el sobrecalentamiento en el reactor nuclear, lo que provoco la explosión de hidrógeno que había acumulado en el interior, la explosión en el cuarto reactor esparció al medio ambiente al menos 200 toneladas de material nuclear. Esta catástrofe nuclear mató a 50 personas y a 300.000 animales de forma inmediata. Pero más tarde hubo 4.000 casos de cáncer, y la zona de Ucrania es aún hoy inhabitable. Ecólogos rusos han señalado que la contaminación radiactiva en los territorios cercanos a la planta nuclear de Chernóbil, en Ucrania, durará más de 300.000 años.
LA MADERA METÁLICA
Desde naves espaciales, aviones y buques de guerra. El titanio se emplea en muchas cosas por ser tan fuerte como el acero pero casi el doble de ligero. Un equipo de las universidades de Pensilvania, Illinois en Urbana-Champaign y Cambridge han construido una lamina de niquel con poros a nanoescala que la hacen tan fuerte como el titanio, pero de cuatro a cinco veces más ligera.Los investigadores lo llaman "madera metálica" porque el espacio vacío de los poros y el proceso de autoensamblaje con el que están hechos hacen que se parezca a un material natural, como la madera.Ese vacío, que alcanza el 70% de la estructura, podría rellenarse con otros materiales.Por ejemplo, uno cargado con ánodos y cátodos le permitiría realizar una doble tarea: un ala plana o una pierna protésica
domingo, 20 de enero de 2019
Desastre del Prestige
El desastre del Prestige más conocido como el CHAPAPOTE fue un derrame de petróleo en Galicia provocado por el hundimiento del buque petrolero Prestige en 2002. El accidente afectó a 2000 kilómetros de costa española, francesa y portuguesa.
El 13 de noviembre de 2002, el petrolero monocasco Prestige se accidentó en una tormenta mientras transitaba cargado con 77 000 toneladas de fuelóleo frente a la Costa de la muerte , en el noroeste de España. Tras varios días de maniobra para su alejamiento de la costa gallega , se acabó hundiendo a unos 250 km de la misma. El vertido de la carga causó una de las catastrofes medioambientales más grandes de la historia de la navegación, tanto por la cantidad de contaminantes liberados como por la extensión del área afectada, una zona comprendida desde el norte de Portugal hasta Francia . El episodio tuvo una especial incidencia en Galicia , donde causó además una crisis política y una importante controversia en la opinión pública.
El derrame de petroleo del Prestige ha sido considerado el tercer accidentes más costoso de la historia , pues la limpieza del vertido y el sellado del buque tuvieron un coste de 12 000 millones de dólares según algunas fuentes, el doble que la explosión del Challenger pero por detrás de la desintegración de Columbia y el accidente nuclear de Chernobyl.
martes, 15 de enero de 2019
BIENVENIDOS
Os doy la bienvenida al blog. Espero que participéis subiendo al menos dos entradas al mes. A la vez pretendo acercaros a la ciencia y hacer el curso más ameno.
Suscribirse a:
Comentarios (Atom)




